针对上述问题,南开大学苏循成教授课题组发展了一种在活细胞内的“可逆加成反应触发的邻基参与”(RAT-NGP)化学反应定点标记蛋白质的方法。该标记化学策略基于一种反应性小分子标签,通过两步连续反应与目标蛋白质(POI-2C)上两个工程改造的、溶剂可及的半胱氨酸残基发生作用。每个功能标签分子含有两个活性基团,其中一个为与游离硫醇可逆反应的Michael受体,另一个则是对硫醇具有特异性反应的可离去基团(LG)。相较于可逆的Michael受体,离去基团对游离硫醇的反应性较低且可调节。在POI-2C中,两个半胱氨酸残基的侧链巯基在空间上具有一定的距离(通常在5-7 Å)。首先,一个游离巯基通过可逆的Michael加成反应与标签分子连接,第一步反应使得标签中的可离去基团(LG)与蛋白质中的另一个巯基更为接近,从而促进巯基对LG的亲核取代反应。第二步反应类似于有机合成中的邻基参与(NGP)反应,在合适的空间距离范围内,两个蛋白质巯基通过级联反应与标签连接,从而实现目标蛋白质的定点标记。该策略的独特之处在于,可逆的Michael加成反应触发了NGP效应,NGP反应进一步稳定了可逆加成产物(见图1),同时有效避免了单一自由巯基的影响,从而实现目标蛋白质的定点标记。
图1. 通过RAT-NGP策略实现蛋白质的位点特异性标记。
为验证RAT-NGP策略对POI-2C进行位点特异性标记的可行性,作者以泛素为模式蛋白,在其α螺旋i, i+4位置引入双半胱氨酸突变,构建了E24C/A28C突变体(POI-2C)。通过通过19F NMR监测T1与POI-2C的反应,结果表明,随着pH值的升高,反应速率也随之增加。在pH 7.5和8.5时,反应分别在22分钟和9分钟内完成。经质谱分析确认只有邻基参与产物T1-POI-2C的生成,并且该产物结构稳定,不受高浓度GSH的影响。通过同位素富集的15N蛋白质样品,作者利用二维15N-HSQC实验详细分析了蛋白质中每个氨基酸残基主链的化学位移在标记前后的变化。研究结果表明,RAT-NGP标记策略对目标蛋白的结构影响极小,几乎未对其三维结构产生扰动。同时,POI-2C与T1结合前后的圆二色光谱(CD)也验证了该标记策略未对蛋白质的二级结构造成明显影响(图2)。
图2. 利用RAT-NPG化学对蛋白质(POI-2C)进行位点特异性标记。
鉴于GSH在细胞内高度丰富且其反应性与溶剂可及的蛋白质巯基相似,作者评估了RAT-NGP标签(T1-T6)对POI-2C相对于GSH的选择性。结果显示,T1对POI-2C的选择性最佳,因而被选为后续研究的功能标签。为了进一步研究RAT-NGP效应对目标蛋白质标记选择性的影响,作者比较了T1对POI-2C(Ub E24C/A28C)和POI-1C(Ub A28C)的反应,发现T1与POI-2C的反应活性比POI-1C高出30倍。这些数据表明邻基参与效应极大地加速了后续不可逆的亲核取代反应。在POI-2C和POI-1C之间的竞争反应中,T1显示出对POI-2C的强烈偏好,甚至在POI-1C过量存在时,T1几乎全部与POI-2C反应。表明RAT-NGP反应对POI-2C相对于GSH和POI-1C具有高选择性(图3)。
图3. RAT-NGP反应对POI-2C相对于GSH和POI-1C的选择性研究。
RAT-NGP策略对蛋白质标记的普适性,通过用一系列分子量差异明显(6-73 kDa)且含有不同数目的天然半胱氨酸的蛋白质进行验证,这些蛋白质包括没有内源半胱氨酸的和有多个半胱氨酸或锌指结构域的蛋白质(图4a)。结果表明,无论目标蛋白质是否含有内源性半胱氨酸,标签T1均能高效(效率≥93%),快速且特异性地与工程化的双半胱氨酸位点反应,而天然半胱氨酸或锌指结构域则完全不受影响,并且人工构建的两个半胱氨酸不但可以在螺旋有序结构区,也可以在柔性较大的环区(loop region)。分子动力学模拟进一步揭示,目标蛋白中的两个半胱氨酸残基之间的硫原子距离在5.8到7.3 Å之间,适合RAT-NGP标记反应。这些结果证明了该策略在不同大小、不同半胱氨酸背景的蛋白质中进行位点特异性修饰的广泛适用性和高效性(图4)。
图4. RAT-NGP定点标记策略应用蛋白质修饰的普适性研究。
该研究证实,T1能有效穿透大肠杆菌及哺乳动物HEK293T细胞膜,在活细胞内实现对目标蛋白质(POI-2C)的高效、位点特异性标记。19F NMR分析显示,T1在大肠杆菌中对POI-2C的标记效率接近100%,在HEK293T细胞中亦可达76%,且该标记对细胞无毒,这对活细胞检测至关重要。该策略条件温和、操作简便,实验中获得的19F-NMR信号清晰可辨,为在活细胞生理环境下进行蛋白质的高分辨率研究提供了有力工具(图5)。
图5. RAT-NGP策略用于活细胞(E. coli和HEK293T)中目标蛋白质的精准标记。
作者还以GB1 A34F蛋白为例,利用RAT-NGP策略结合高分辨率19F NMR技术在活细胞中研究了蛋白质二聚化。实验结果表明该蛋白质在活细胞中主要以二聚体形式存在。而细胞裂解后,因蛋白浓度稀释导致二聚化程度显著下降。该方法成功应用于监测活细胞中蛋白质二聚化过程,证明了其在研究蛋白质-蛋白质相互作用的高分辨研究潜力(图6)。
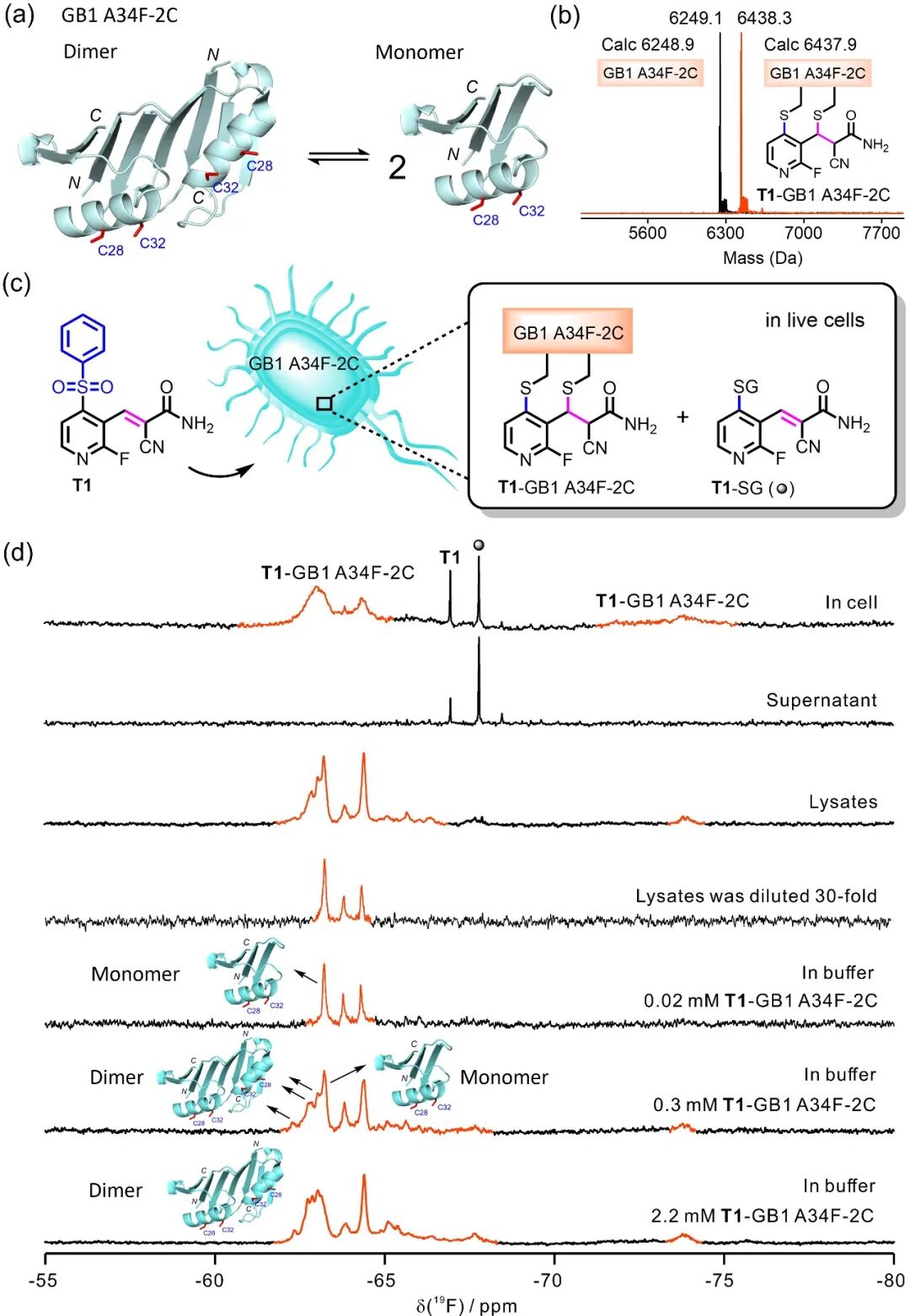
图6. RAT-NGP策略用于活细胞中蛋白质二聚化测定。
总结与展望:
综上所述,本研究展示的RAT-NGP策略,仅需在目标蛋白质上人为引入两个具有一定空间距离的半胱氨酸残基,无需突变内源性半胱氨酸,就能在体外和活细胞中实现目标蛋白质的位点精准与高效标记。该方法在体外与活细胞中均表现出优异的标记效率与选择性,对内源性半胱氨酸无干扰,且对细胞无毒害。借助19F NMR技术,研究成功将该策略应用于活细胞内蛋白质二聚化的高分辨分析。该策略为活细胞中蛋白质结构、相互作用与动态的高分辨研究提供了有力工具。随着CRISPR技术的进步,可以在基因组中精确插入两个溶剂可及的半胱氨酸残基,RAT-NGP标记方法使得在目标蛋白质中定点引入官能团成为可能,同时对蛋白质三维结构的扰动微乎其微,这为活细胞研究带来了巨大的应用前景。这些官能团可包括用于研究目标蛋白质动态、相互作用及关联的磁性探针、荧光传感器等。
该研究成果以“Efficient Precision Labeling of Proteins in Live Cells via Highly Selective Thiol-Chemistry Illustrated by In-Cell 19F-NMR”为题,以Research Article的形式发表在CCS Chemistry。南开大学的苏循成教授为论文的通讯作者,博士后郭书丽、博士研究生李斌和张兴为论文共同第一作者。该工作获得中国科学院战略性先导科技专项、科技部和国家自然科学基金的支持。