大家好,今天给大家介绍的文章是最近发表在Angew 上的Efficient Protein-Protein Couplings Mediated by Small Molecules under Mild Conditions,文章的通讯作者是南开大学的苏循成教授。
开发生理条件下高效的蛋白质-蛋白质偶联方法以保持蛋白质的三维结构和功能是非常重要的。最近的研究表明,苯磺酰吡啶衍生物可以与巯基发生取代反应,而N端半胱氨酸与醛基环化形成噻唑烷则是修饰蛋白质的有效方法。受到这些研究的启发,作者开发了一个使用5-氟-4(苯基磺酰基)吡咯醛(FPPA)介导的蛋白质偶联方法。在FPPA中,苯磺酰和醛的吸电子作用提高了氟与游离硫醇的取代反应活性,使其明显高于苯环酰基。
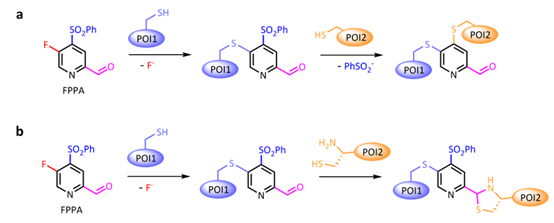
图1. 两种FPPA介导的蛋白质偶联模式
作者概述了两种由FPPA介导的蛋白质偶联方法(图1)。一种为两次芳香亲核取代反应,第二种为取代反应加N端半胱氨酸与醛基环化反应。FPPA介导的高效蛋白质-蛋白质偶联已在许多蛋白质中得到证实,此外作者还实现了三种生物分子的三脚架型的偶联方式。
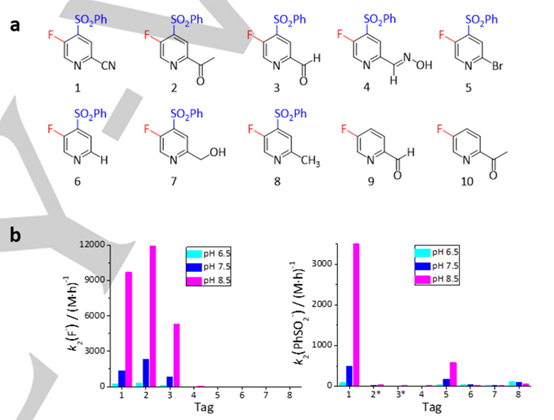
图2. 不同取代基的芳香烃与巯基的反应
作者首先验证了小分子模型反应,合成了具有不同取代基的含氟芳香烃(图2a)。作者发现化合物1-4可以与巯基发生F的取代反应而5-10不能发生,说明在该反应中磺酰基以及醛基的吸电子效应至关重要。作者也发现取代反应速率随着pH值升高而上升(图2b)。化合物4的F取代速率较低,而化合物1中F取代以及苯磺酰取代反应速率比较低,不能体现选择性。考虑到醛后续可以与N端半胱氨酸环化,作者最终选择使用化合物3(FPPA)作为偶联试剂。

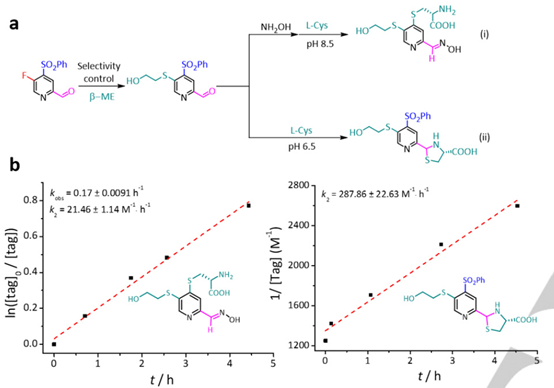
图3. 两种偶联模式的小分子模型反应
作者随后验证了FPPA的小分子模型反应。作者发现在羟胺保护、pH为8.5时,半胱氨酸可以与苯磺酰基发生取代反应。而在pH为6.5时,半胱氨酸可以专一地与醛基发生环化反应(图3)。
作者接着评估了多种蛋白的FPPA介导的偶联反应。首先是巯基双取代的反应模式(图3a i),作者使用了两种泛素半胱氨酸突变体K63C和G76C对该反应进行验证(图4)。在室温、pH为7.5以及两当量FPPA的条件下,Ub K63C的巯基完成了F的取代反应,未观察到其他副反应。而后续与Ub G76C的取代中,作者发现使用羟胺保护或直接反应产率均低于50%(图4b)。作者后续加入了TECP还原剂,可以将转化率提高至60%。
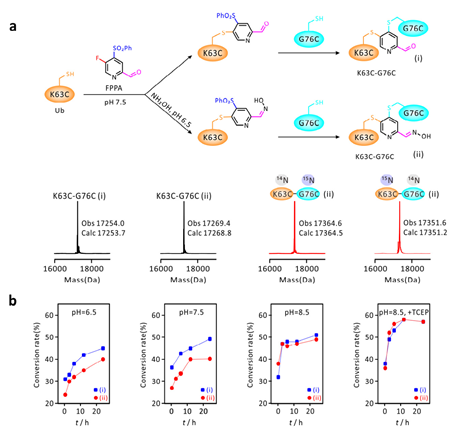

图4. 通过巯基双取代反应实现泛素偶联
作者随后评估了第一步发生巯基对F的亲核取代,第二步发生环化反应的偶联模式(图3a ii)。作者使用XIAP蛋白中的BIR3结构域作为POI1,UBA结构域作为POI2进行了偶联反应(图5)。结果显示BIR3的第一步取代反应定量转化而该结构域中与Zn2+结合的三个半胱氨酸未被修饰。BIR3_PPA与N端半胱氨酸的UBA在pH为6.5的条件下在2h内也完成了醛的环化反应。作者还发现该环化反应快与半胱氨酸小分子与醛的环化反应,作者认为这是由于蛋白质中伯胺pKa的降低使得亲核反应速率增加。

图5. BIR3与UBA结构域通过FPPA介导的偶联
作者最后进行了三种生物分子三脚架型的偶联尝试。作者分别使用两种策略(图6),即先苯磺酰基取代后醛基环化或顺序相反,最终发现先取代后环化的方式可以得到更高的转化率(45%)。FPPA介导的在生理条件下蛋白质间的三重偶联是制药工业和蛋白质化学领域中一种新的方法,生成的偶联物中三个部分通过刚性的苯环连接。作者后续也验证了偶联物的稳定性以及偶联反应对蛋白质的三维结构几乎不产生影响。
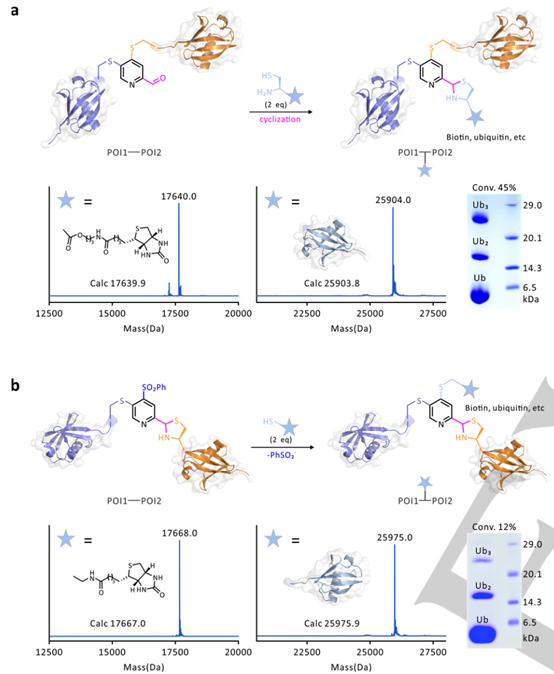

图6. FPPA介导的三分子偶联反应的两种途径
综上所述,作者设计合成了一种FPPA小分子。在温和条件下可以首先发生游离巯基与氟的高效取代反应,随后再和另一分子的巯基发生苯磺酰基的取代反应或与N端半胱氨酸发生醛基的环化反应,从而实现蛋白质之间的偶联反应。FPPA也能够以三脚架的方式实现三个大分子的偶联反应。该体系中反应均可以在生理条件下发生并且对蛋白的三维结构不产生影响。
作者:WLT 审校:DYH
DOI: 10.1002/anie.202205597