稀土离子具有很强的Lewis酸性,因此具有独特的反应性。特别是稀土催化的不饱和化合物的氢元素化反应展示出不同于过渡金属的选择性及反应性。近期,南开大学崔春明课题组利用烯基-二胺稀土催化体系实现了内烯烃的硅氢化反应 (ACS Catal. 2018, 8, 2230),以及内炔烃的双硅氢化反应 (Angew. Chem. Int. Ed. 2020, 59, 2365)。1,3-烯炔含有共轭的烯烃和炔烃单元,具有易制备、结构多样和反应性丰富等特点,是有机合成中重要的合成砌块。然而,1,3-烯炔的催化硅氢化反应面临着区域和立体选择性控制的问题,存在三种主要的竞争途径,即1,2-、1,4-和4,3-加成途径。然而,催化1,3-烯炔的1,4-硅氢化反应只有几例报道,且底物范围非常有限。该课题组在前期稀土催化硅氢化的基础上,使用阴离子型稀土配合物为催化剂,首次实现了支链1,3-烯炔的高效选择性1,4-硅氢化反应,在温和的反应条件下得到多种四取代硅基联烯。其中,稀土离子半径以及ate结构对反应起决定性作用。此外,结合氘代实验、动力学实验和DFT计算,提出了稀土催化1,3-烯炔的1,4-硅氢化的配位插入和σ-键复分解反应机理。
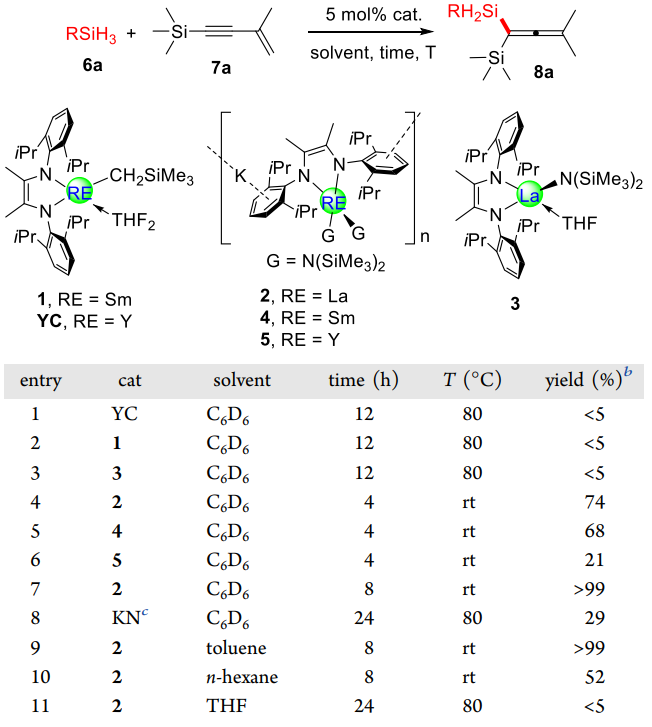
研究人员首先对催化剂和反应条件进行优化。当采用中性稀土催化剂YC,1和3时 (entries 1−3),即使在80 ℃加热条件下反应12 h,也仅只有极低的转化率 (< 5%)。而当采用烯基二胺配体稀土双胺基钾盐2、4及5为催化剂时,室温反应4 h即能观察到有一定量的区域选择性硅氢化产物8a生成 (entries 4−6)。其中,室温4 h条件下,催化剂2以74%的高产率得8a,催化剂4和5为68%和21%。这展示了稀土离子半径对催化硅氢化反应的调控作用,离子半径越大,催化剂活性越高。胺基钾盐KN(SiMe3)2也具有活性 (entry 8),但即使加热至80 ℃反应24小时后也只有29%的产率,继续延长反应时间没有明显变化。

研究人员对催化反应的底物适用范围进行了研究。在优化的条件下,以5 mol%量的配合物2为催化剂,以甲苯为溶剂研究了硅烷 (nC6H13SiH3, CySiH3及多种芳基硅烷) 与各种1,3-烯炔的1,4-硅氢化反应。所有的烯炔都经过1,4-硅氢化以高产率 (83−94%) 得到四取代双硅基联烯8a−r,而其他硅氢化产物 (4,3-加成, 1,2-加成等) 在1H NMR和GC-MS谱图均未观察到。当1,3-烯炔的硅基连于三键时 (R1 = silyl),反应得到偕二硅基联烯产物8a−g,产率为85−91 %;当硅基连于双键时 (R2 = silyl),反应得到1,3-二硅基联烯产物8h−r,产率为83−94 %。值得注意的是,该反应对具备较大的空间位阻的底物也可能以高产率顺利得到硅氢化产物。长链烷基烯炔的反应也可以顺利进行,得到四取代联烯。对于含叔丁基二甲基硅氧基的烯炔,需要较长的反应时间 (16h) 才能以满意的产率得到硅氢化产物。另一方面,硅烷的空间效应也影响反应速率,与正己基硅烷相比 (rt, 8h),环己基硅烷6b对1,3-烯炔的硅氢化反应速率更低,需要更高温度和更长反应时间 (60 °C, 16h) 才能以高产率得到目标产物。
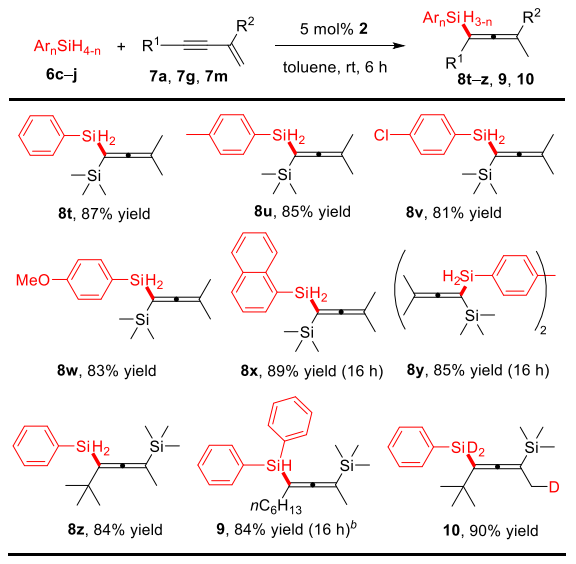
研究发现,芳基硅烷也可用于1,3-烯炔的高效催化硅氢化反应,以高产率 (81−90%) 得到四取代双硅基联烯8t−z,同时具有专一的区域选择性。该反应能耐受含有氯和烷氧基的硅烷。另外,以4,4'-二硅基联苯二硅烷为硅氢化试剂,可以得到二联烯8y。值得注意的是,硅烷的取代基对催化活性影响显著:芳基硅烷通常比烷基硅烷 (正己基和环己基) 活性高,而位阻较大的硅烷的活性较低 (萘基)。
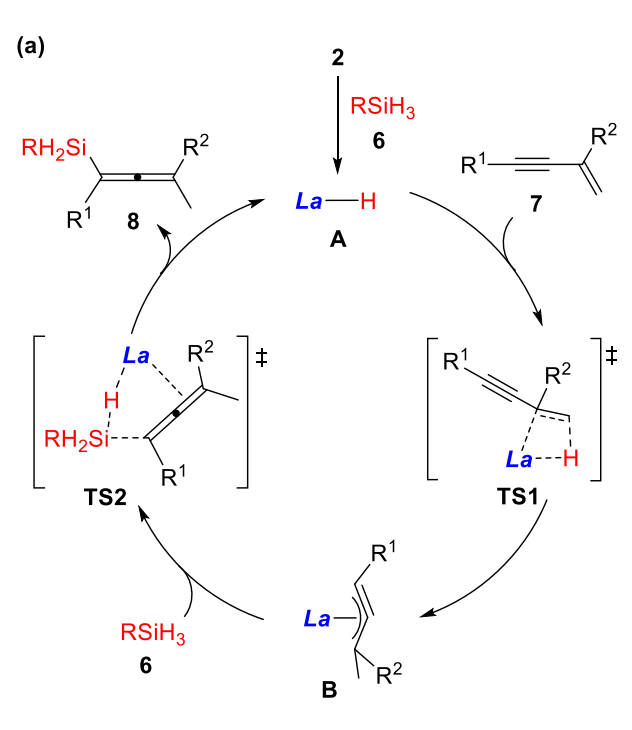
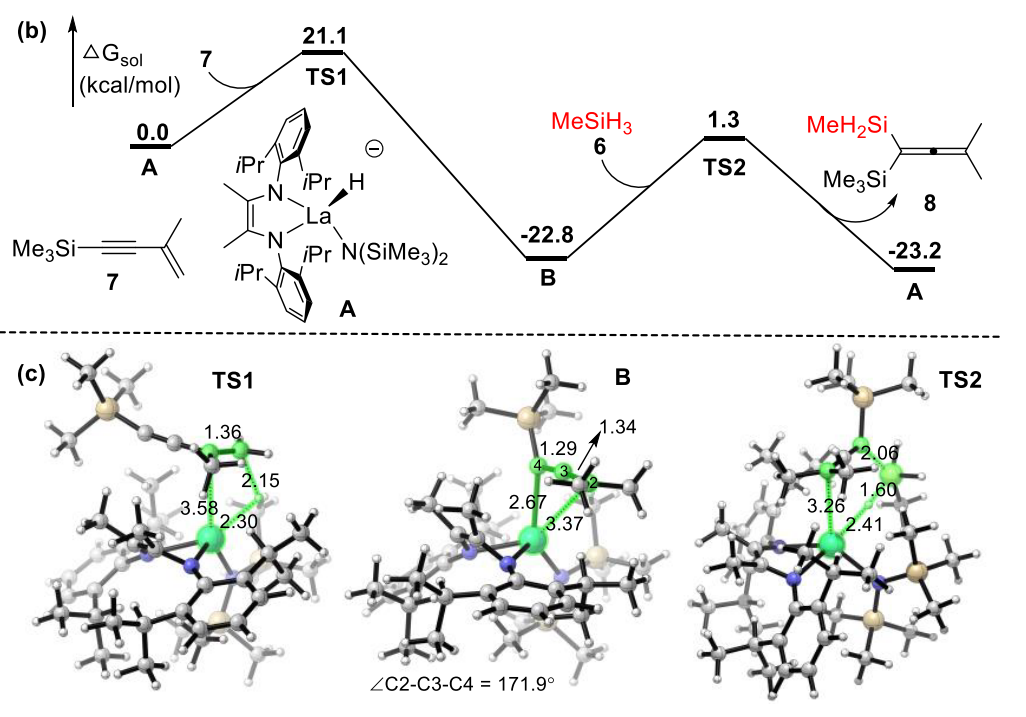
结合课题组前期的机理研究,研究人员认为稀土催化1,3-烯炔的1,4-硅氢化反应机理应如图所示。首先,烯基-二胺配体稀土双胺基钾盐与硅烷反应产生阴离子稀土氢化物A。之后,A对烯炔双键末端位点进攻形成η3配位的炔丙基镧中间体B。最后,B与硅烷发生σ-键复分解形成硅基联烯产物及稀土氢化物,完成催化循环。
该成果发表在JACS上(J. Am. Chem. Soc. 2021, 143, 12913–12918)。通讯作者为南开大学崔春明教授,李建峰副教授为共同通讯作者,博士研究生陈武丰为第一作者。该工作的理论计算部分得到许秀芳教授和姜春卉的帮助。上述工作得到国家自然科学基金的资助。
文章链接:https://pubs.acs.org/doi/10.1021/jacs.1c04689