过渡金属氢化物(MH)催化的烯醇/烯醇式与不饱和烃的偶联反应,是一种原子经济性C-C键形成策略,受到越来越多的关注。这些反应是从M-H加成到不饱烃形成亲电性的π-烯丙基金属中间体启动的,再与可烯醇化的羰基化合物反应生成C-C键(图1A)。虽然这些反应的不对称版本已经取得了进展,但当用这些方法产生两个相邻的手性中心时,立体化学控制仍然极具挑战。Dong Vy课题组报道了迄今为止唯一成功的案例,开发了一种由Rh-H和Jacobsen胺组成的协同体系,实现了醛与炔的立体多样性偶联。在此基础上,结合近年来Ir-催化的立体多样性烯丙基烷基化反应的研究进展,南开大学资伟伟研究员课题组报道了1,3-二烯类化合物与醛亚胺酯在Pd-和Cu-协同催化下的不对称偶联反应,利用这两种催化剂不同对映体的组合,可以区域选择性、非对映选择性及对映选择性地得到四种可能的立体异构体,文章近日发表于J. Am. Chem. Soc.上,DOI:10.1021/jacs.9b07600。
Malcolmson等人的开创性工作表明,Pd-膦噁唑啉(Pd-PHOX)催化剂可用于各种活化的C-前亲核试剂对1,3-二烯的高对映选择性的加成,但没有评估弱亲核性的前亲核试剂如氨基酸衍生物。周其林院士等人报道了Ni(0)催化的1,3-二烯与简单酮的偶联反应,但当生成两个手性中心时,得到了近1:1的非对映体混合物。这可能是由于第二个过渡金属活化亲核试剂时不仅会扩大反应的范围,而且对反应性弱的亲核试剂,如醛亚胺酯类,也会提供对立体化学的额外控制。因此,资伟伟课题组设计了一个具有两个催化循环的立体选择性C-C偶联反应体系,每个反应都涉及不同的过渡金属。
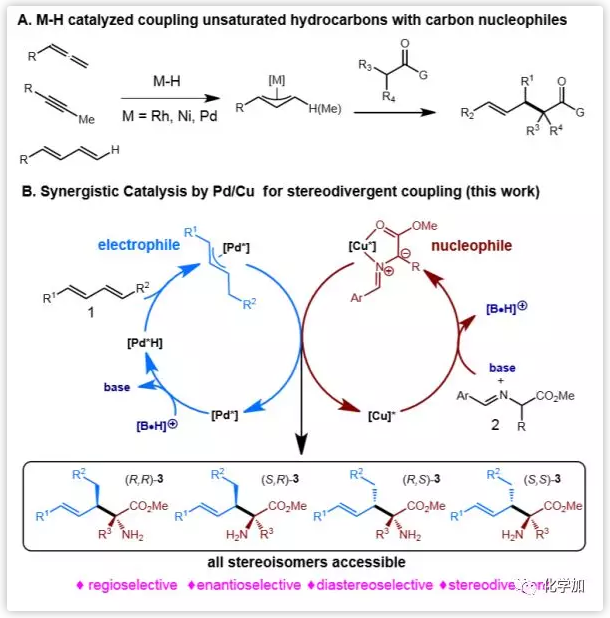
图1. Pd-和Cu-协同催化策略(图片来源:J. Am. Chem. Soc.)
醛亚胺酯由于其在环加成反应、烯丙基烷基化等不对称转化过程中具有良好的立体控制作用,因而被选为亲核试剂。最近,张万斌课题组和王春江课题组分别报道了π-烯丙基钯物种能够在强碱条件下与铜络合的氮杂亚甲基叶立德反应,立体选择性地得到烯丙基化产物。在本文的体系(1B)中,作者设想在合适的碱和过渡金属如Cu的作用下,金属化氮杂亚甲基叶立德将作为亲核试剂与由Pd-H介导的1,3-二烯类迁移插入生成的亲电性π-烯丙基Pd中间体反应。Pd-H由Pd(0)物种与质子化的Brønsted碱反应生成,该碱可同时再生Brønsted碱,参与Cu-催化循环。Cu-和Pd-催化剂分别决定了亲核试剂和亲电试剂的构型,从而能够在偶联过程中控制产物3的两个立体中心的构型。也就是说,使用两种手性催化剂的不同组合,即PdR+CuR、PdS+CuR、PdS+CuS和PdR+CuS可以获得所有四种可能的立体异构体。
首先,作者在30 °C下以1,3-二烯1a和丙氨酸衍生的醛亚胺酯2a为模型底物,Et3N为碱,Pd-PHOX配合物Pd-1为催化剂,进行了初步实验(图2)。当Cu(I)与膦基二茂铁噁唑啉配体(S,SP)-L1活化醛亚胺酯时,得到了理想的偶联产物3aa,产率为53%。虽然非对映体选择性较差(dr=1.6:1),但主要立体异构体的ee值为95%。Et3N的选择是反应的关键,强碱如Cs2CO3和DBU未能给出所需的产物,大位阻碱,如iPr2NEt,DABCO能催化这一反应,但转化率极低。

图2. 反应条件优化(图片来源:J. Am. Chem. Soc.)
将Cu(I)配体切换到(S,SP)-L2时得到了较好的产量和略高的dr。对一系列双膦衍生的Pd-配合物考察显示Josiphos衍生的Pd-6给出了最佳结果。当使用Cu(I)/ (S,SP)-L2和Pd-6的组合时,以88%的产率得到(2S,3R)-3aa,为单一立体异构体,对映选择性和非对映体选择性优异(>99%ee,>20∶1dr)。相反地,用(R,RP)-L2代替(S,SP)-L2作为Cu(I)配体时,对映体选择性完全逆转:以83%的收率得到(2R,3R)-3aa,dr值为14∶1,ee 值>99%。对照试验显示Pd-和Cu-催化剂都是必不可少的。
为了测试这种偶联的立体多样性,作者在Pd-和Cu-催化剂的四种不同组合下进行了1a和2a的反应。如图3所示,均能以良好的产率获得3aa的四种立体异构体,且具有优良的对映选择性和非对映选择性。结果表明,一个催化剂在偶联过程中控制亲电性烯丙基的立体化学,另一个控制亲核性烯醇式的立体化学。

图3. 立体多样性合成3aa的四种异构体(图片来源:J. Am. Chem. Soc.)
接下来,作者考察了1,3-二烯的底物范围(图4)。R基可以是一个含缺电子、电中性或富电子取代基的苯环,取代基的位置对反应结果影响不大。在所有情况下,都得到了相应的产物(3ba-3ia),产率中等至良好,具有优异的对映选择性和非对映选择性。其它芳香环(萘[3ja]、呋喃[3ka]、噻吩[3la]和吲哚[3ma])的底物在标准条件下反应良好。对于烷基取代的1,3-二烯,虽然产物(3na)的dr>20:1,ee为93%,但产率较低。3ga的绝对构型经单晶X-射线分析确定为(2S,3R)。
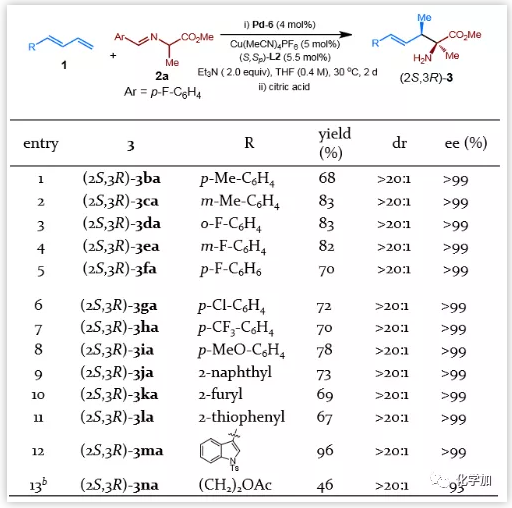
图4. 1,3-二烯的底物范围(图片来源:J. Am. Chem. Soc.)
随后,作者考察了醛亚胺酯的范围(图5)。从天然和非天然α-氨基酸衍生出的醛亚胺都是1,3-二烯1a的适宜偶联配偶体。值得注意的是,含有额外配位位点(酯[3ag]、胺[3ah]、甲基硫化物[3ai]和烯烃[3aj])的底物具有良好的耐受性。谷氨酸衍生的醛亚胺酯也能顺利反应,但在酸性处理过程中,得到了内酰胺3ak。对内酯和环亚胺的衍生醛亚胺酯进行测试,发现它们分别得到了相应的环状产物3al和3am,且具有良好的立体选择性。作者还改变了醛亚胺的酯基,乙酯、异丙酯和叔丁酯都反应顺利,相应产物的dr>20:1,ee>99%。大位阻酯基的存在略微提高了产率(比较3an、3ao和3ap的产率),这可能是因为空间位阻减少了起始醛亚胺在反应过程中的水解。

图5. 醛亚胺酯的范围(图片来源:J. Am. Chem. Soc.)
在考察了这种偶联反应的底物范围后,作者探讨了它的立体多样性(图6)。为此,用单独的Pd-6对映体和两个L2-Cu对映体进行反应。在此条件下,3ab、3ca、3da、3fa、3ja和3am的对映体均以优良的产率得到,且具有优良的非对映选择性和对映选择性。从甘氨酸酯衍生出的醛亚胺的反应有可能获得双偶联产物,因此作者用一种大位阻的酮亚胺代替醛亚胺,以阻止第二次偶联反应。例如,在不改变标准反应条件的情况下,合成了3aq和3eq,两种非对映异构体的产率优良,均具有>20:1的dr值和>99%的ee值。
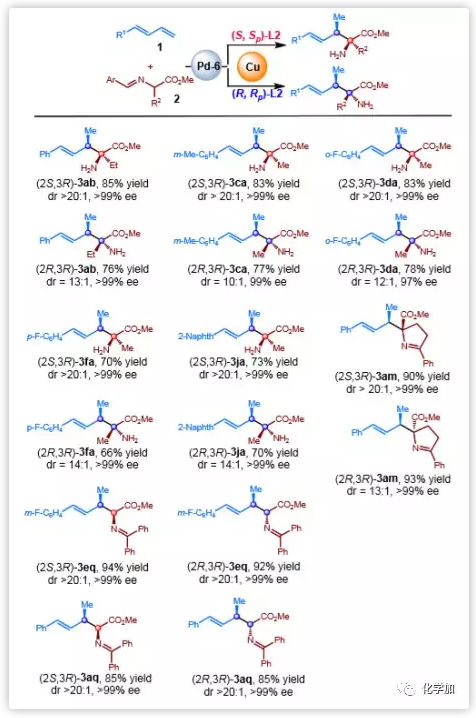
图6. 立体多样性合成(图片来源:J. Am. Chem. Soc.)
亲核试剂对1,4-二取代二烯的加成极为罕见,因为它们的反应活性很低,并且区域选择性控制极具挑战。因此,作者也用一些带有芳基和烷基的内部1,3-二烯来测试该方法(图7)。这些二烯的产率和非对映选择性均低于端二烯,但在三种情况下对映选择性都良好。此外,区域选择性被完全控制,加成反应完全发生在烷基取代位点。最后,用这些内部1,3-二烯也可以实现立体多样性的反应。该结果表明,用作者的方法可以很容易地得到具有两个相邻手性中心(在α-和β-位)的合成有用的氨基酸酯的四种可能的立体异构体。
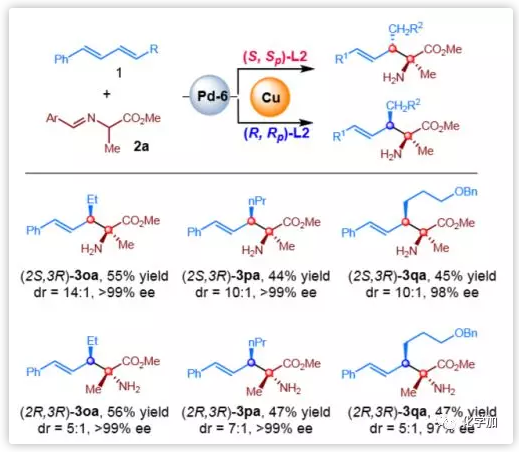
图7. 内部1,3-二烯的立体多样性偶联(图片来源:J. Am. Chem. Soc.)
总结:南开大学资伟伟课题组报道了一种在Pd-和Cu-协同催化下,1,3-二烯与醛亚胺酯的立体多样性偶联反应。该方法具有广泛的底物范围,可以通过改变两种手性金属催化剂的构型来制备具有优秀非对映选择性和对映选择性的两个相邻手性中心(α-和β-)的合成有用的氨基酸酯的所有四种可能的立体异构体。该项工作也为其它与Pd-H相关的协同催化提供了理论依据。